摘要:介绍了据本厂水质所摸索出的测定化学需氧量的新的方法,及用此方法做实验所得结果的可行性。
关键词:化学需氧量 重铬酸钾 废水
新沂市城市污水处理厂位于新沂市南郊,占地面积6.6万平方米,担负着城区污水的收集和处理任务。其废水来源主要有以下几种途径:一、市内居民生活污水;二、部分处理后的工业废水;三、上游地区废水排入淮江支流后引起的水污染。近年来,随着城乡建设和经济建设的不断发展,工业和生活污水量不断增加,尤其工业废水的不断增加使进水水质严重恶化,而工业废水中氯离子浓度的增加对化学需氧量的测定影响较大。
本测定方法针对上述情况,结合我厂实际水质对传统COD测定法进行了改进,克服了传统的加入0.4g硫酸汞以消除氯离子的干扰中剧毒硫酸汞对环境和人体危害较大的情况。
1.测定原理
用高浓度的硝酸银对水样中的氯离子进行滴定以掩蔽氯离子并且利用氯化银的溶解度小于重铬酸银的原理,以生成的砖红色重铬酸银沉淀来指示滴定终点。然后在强酸性溶液中,一定量的重铬酸钾氧化水样中还原性物质,过量的重铬酸钾以试亚铁灵作指示剂,用硫酸亚铁铵溶液回滴。根据用量算出水样中还原性物质消耗氧的量。
2.仪器及试剂
2.1 仪器
1) 回流装置:带250ml磨口锥形瓶的全玻璃回流装置
2) 加热装置:变阻电炉
3) 50ml酸式滴定管
2.2 试剂
1)重铬酸钾标准溶液(1/6K2Cr2O7=0.2500mol/L):称取预先在120℃烘干2h的基准或优级纯重铬酸钾12.258g溶于水中,移入1000ml容量瓶中,稀释至标线,摇匀。
2)试亚铁灵指示液:称取1.485g邻菲罗啉(C12H8N2·H2O,1,10—phenanthnoline),0.695g硫酸亚铁(FeSO4·7H2O)溶于水中,稀释至100ml,贮于棕色瓶内.
3)硫酸亚铁铵标准溶液((NH4)2Fe(SO4)2·6H2O=0.1mol/L):称取39.5g硫酸亚铁铵溶于水中,边搅拌边缓慢加入20ml浓硫酸,冷却后移入1000ml容量瓶中,加水稀释至标线,摇匀.临用前,用重铬酸钾标准溶液标定.
4)硝酸银溶液(100g/L):称取100g硝酸银(分析纯)溶于蒸馏水并稀释至1000ml.贮于棕色瓶中
5)硫酸--硫酸银溶液:于500ml浓硫酸中加入5g硫酸银,放置1-2天,不时摇动使其溶解。
6)氯化钠溶液:称取1g溶于1000ml水中.
3.测定步骤
1)取20.00ml混合均匀水样(或适量水样稀释至20.00ml)置250ml磨口的回流锥形瓶中,准确加入10.00ml重铬酸钾标准溶液
2)用硝酸银溶液对上述水样进行滴定至出现砖红色沉淀.
3)随后加入数粒小玻璃珠至上述水样中,连接磨口回流冷凝管,并从冷凝管上口慢慢地加入30ml硫酸--硫酸银溶液,轻摇锥形瓶使之混匀,加热回流2h(自开始沸腾时记时)
4)冷却后,用90ml水冲洗冷凝管壁,取下锥形瓶.溶液再度冷却后,若仍然发现有砖红色沉淀则加入数滴氯化钠溶液(1g/L)直至砖红色沉淀消失.
5)上述水样中加3滴试亚铁灵指示液,用硫酸亚铁铵标准溶液(0.1mol/L)滴定,溶液的颜色由黄色经蓝绿色至红褐色即为终点,记录硫酸亚铁铵标准溶液的用量.
6)测定水样的同时用20ml重蒸馏水按同样操作步骤作空白试验,记录硫酸亚铁铵标准溶液用量.
4.计算:
COD = ( V0 - V1 ) × C × 8 × 1000/V
式中 V0 ------- 滴定空白时硫酸亚铁铵标准溶液用量,mg/L
V1 ------- 滴定水样时硫酸亚铁铵标准溶液用量,mg/L
C------- 硫酸亚铁铵标准溶液的浓度,mol/L
V------- 水样的体积,ml
5.测定结果
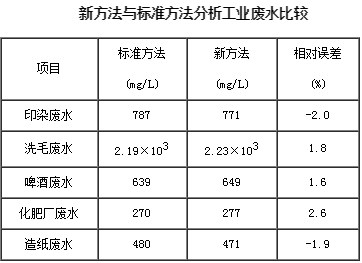
分析经迧处理的浓度为208mg/L的标样(加入了氯化钠使各水样氯离子的含量分别为50、200、1000、4000mg/L)。结果显示,测定标准偏差为0.7%-1.8%,相对误差为-0.2%-0.9%.该方法与标准方法分析结果对照见表.
6.讨论
1)新方法的优点在于不需使用剧毒药品硫酸汞,避免了使用硫酸汞所造成的对人的危害和对环境的二次污染.测定结果在容许误差范围内.
2)出现的沉淀或多或少会造成滴定终点不明显,使测定结果不精确.
3)实验中若砖红色沉淀不消失,必然会使消耗的重铬酸钾用量加大,故滴定前一定要加氯化钠使砖红色沉淀消失.
参考文献:
国家环俽局.水和废水监测分析方法(M).北京:中国环境出版社.1998
